Interpretación el espectro infrarrojo
La interpretación del espectro infrarrojo es como leer un código de barras para identificar qué moléculas hay en una sustancia.
Cuando la luz infrarroja pasa a través de una muestra, algunas frecuencias son absorbidas y otras no. Esto crea un gráfico (espectro) con picos que indican cómo vibran los enlaces químicos en la molécula.
Cada tipo de enlace (como C-H, O-H, C=O) absorbe en una zona específica del espectro. Comparando los picos con tablas conocidas, se puede identificar qué grupos funcionales tiene la molécula y, en algunos casos, de qué sustancia se trata.
Interpretar un espectro infrarrojo es como resolver un rompecabezas: cada pico o banda en el gráfico nos da una pista sobre las moléculas presentes en la muestra.
Pasos para interpretar un espectro infrarrojo:
Observar el espectro: Mira el gráfico, que tiene dos ejes
Eje X (horizontal): Representa el número de onda (en cm⁻¹), que indica la frecuencia de la luz infrarroja absorbida.
Eje Y (vertical): Representa la absorbancia, que nos dice cuánta luz infrarroja ha sido absorbida.
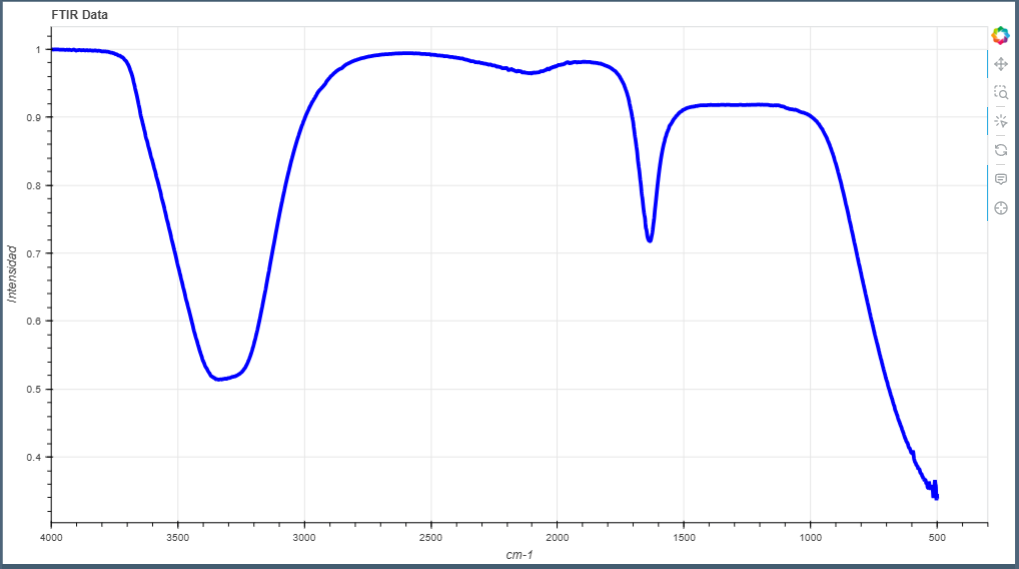
Identificar las regiones clave: Divide el espectro en regiones importantes:
4000-2500 cm⁻¹: Aquí aparecen los estiramientos de enlaces como O-H (agua, alcoholes) y N-H (amidas).
2500-2000 cm⁻¹: Aparecen estiramientos de enlaces triples, como C≡C (alquinos) o C≡N (nitrilos).
2000-1500 cm⁻¹: Aquí se ven estiramientos de enlaces dobles, como C=O (carbonilos) y C=C (alquenos).
1500-500 cm⁻¹: Es la "región de las huellas dactilares", donde aparecen vibraciones complejas y flexiones que son únicas para cada molécula.
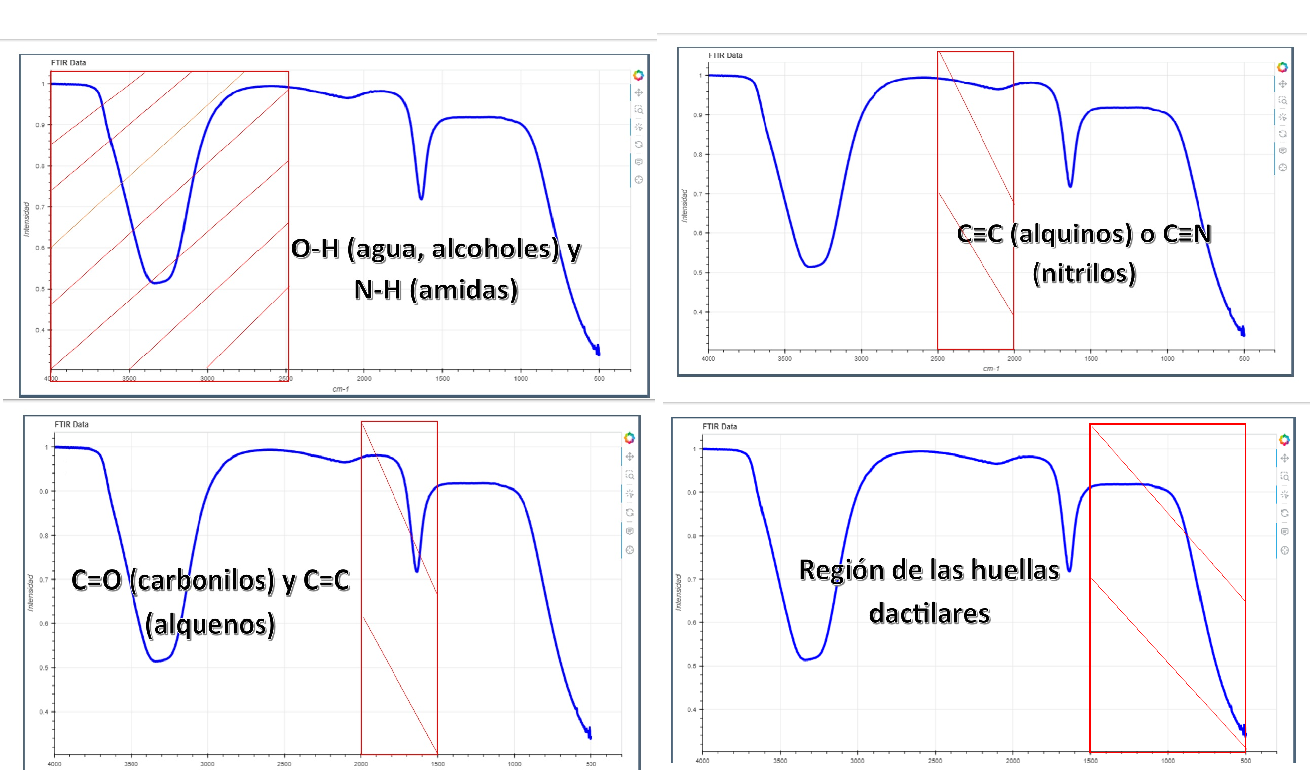
Buscar bandas de absorción: Localiza los picos (bandas de absorción) en el espectro. Cada pico corresponde a la absorción de luz infrarroja por un enlace o grupo funcional específico.
Comparar con tablas de referencia: Usa tablas de referencia para identificar qué grupos funcionales absorben en cada número de onda.
Un pico en 1700 cm⁻¹ sugiere un grupo carbonilo (C=O).
Un pico en 3300 cm⁻¹ puede indicar un grupo hidroxilo (O-H) o amino (N-H).
Analizar la forma e intensidad de los picos:
La intensidad (altura del pico) nos dice cuánta luz ha sido absorbida. Picos altos indican absorción fuerte.
o La forma del pico también es importante. Por ejemplo, un pico ancho en 3300 cm⁻¹ suele ser un grupo O-H (como en alcoholes o agua).
Identificar la molécula: Combina toda la información (frecuencias, intensidades y formas de los picos) para identificar las moléculas presentes en la muestra. Por ejemplo:
Si ves un pico en 1700 cm⁻¹ y otro en 2900 cm⁻¹, podrías estar frente a una cetona (C=O) y un hidrocarburo (C-H).
Confirmar con otros datos:
Si es posible, compara el espectro con bases de datos o espectros conocidos para confirmar tu interpretación.
