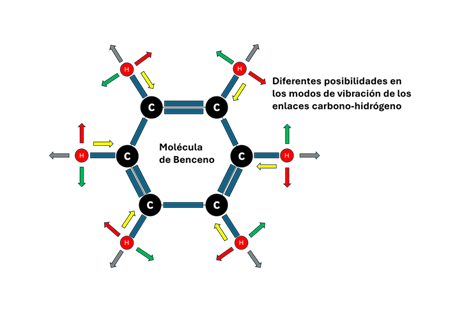
MODOS DE NORMALES DE VIBRACIÓN
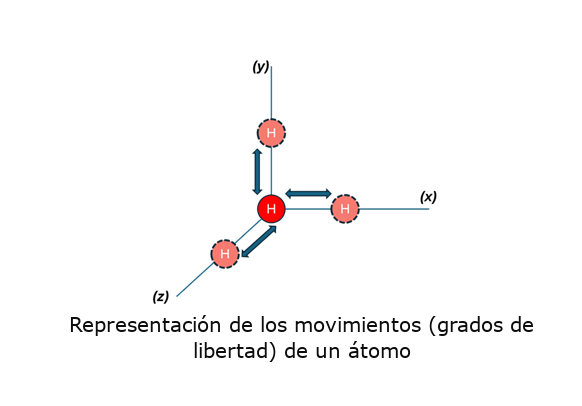
La interacción de la radiación infrarroja con una muestra se puede entender observando los cambios en los momentos dipolares que ocurren durante las vibraciones y rotaciones de los átomos que conforman las moléculas. Cada átomo dentro de una molécula tiene tres grados de libertad, ya que puede moverse en las direcciones de los ejes x, y y z. Cuando una molécula vibra de forma natural, lo hace a una frecuencia específica. Si una radiación infrarroja incide sobre la muestra y su frecuencia coincide con la frecuencia de esa vibración, se produce una resonancia. Esto intensifica la vibración del enlace afectado y genera un cambio más marcado en su momento dipolar. Además de vibrar, las moléculas también pueden experimentar movimientos de rotación o traslación, aunque en el caso del infrarrojo, lo que se detecta principalmente son las vibraciones que provocan cambios en el momento dipolar. Estos cambios son los responsables de que ciertas frecuencias de la radiación infrarroja sean absorbidas por la muestra, lo cual se traduce en la aparición de bandas características en el espectro.
En general, las vibraciones pueden ser como aquellas que cambian longitudinalmente sus enlaces (estiramiento) o que cambien de ángulo sus enlaces (flexión). Algunas de las vibraciones de estiramiento pueden ser de dos tipos, en fase (estiramiento simétrico) o fuera de fase (estiramiento asimétrico).
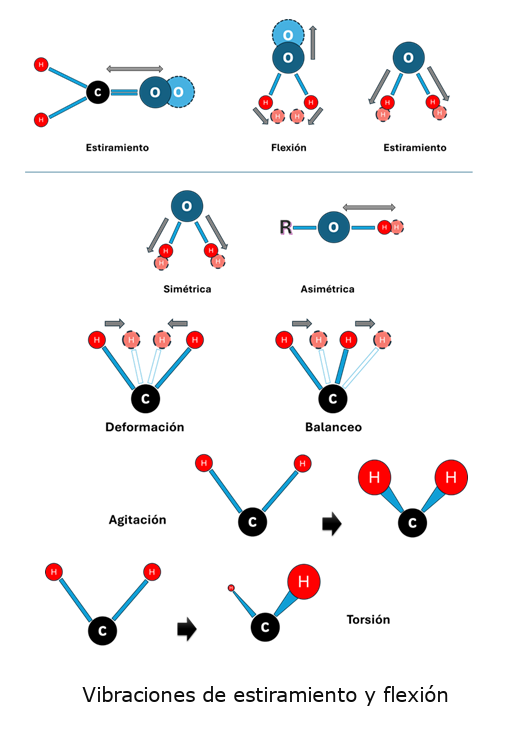
En una molécula, los átomos pueden vibrar de diferentes maneras, conocidas como modos normales de vibración. Estos incluyen vibraciones de flexión, que pueden clasificarse como: a) dentro del plano: deformación y balanceo. b) Fuera del plano: agitación y torsión. En moléculas simples, como el agua, estos movimientos son más evidentes. Sin embargo, en moléculas más complejas, donde los átomos están interconectados rígidamente, estas vibraciones se ven afectadas por la estructura de la red molecular. El número total de modos normales de vibración depende del número de átomos (n) de la molécula: para moléculas no lineales: 3n – 6 y para moléculas lineales: 3n – 5
Por ejemplo, en la molécula de agua (H₂O), se observan tres modos normales: a) Estiramiento simétrico (≈ 3500 cm⁻¹), b) Estiramiento asimétrico (≈ 3400 cm⁻¹), c) Flexión angular (≈ 1600 cm⁻¹).
No todas las moléculas presentan los mismos valores de frecuencia para un mismo tipo de vibración (como la tensión simétrica), ya que estos dependen de las masas atómicas y la fuerza de los enlaces. Cada molécula posee una energía de vibración característica, que puede aumentar si absorbe radiación infrarroja. Al hacerlo, la molécula no cambia el tipo ni la frecuencia de vibración, pero sí aumenta la amplitud del movimiento, pasando a un estado vibracional más alto.